毒蛇、凝胶、激光笔……你确定是在讨论伤口愈合吗?
来源:新浪科技综合 2021-11-03 10:47:33
来源:我是科学家iScientist
日本动漫《工作细胞》里萌翻了的怪力萝莉,拟人化的是我们人体血液中具有凝血作用的血小板。
当血管受伤后,身体的第一反应就是让血管壁肌肉收缩,使受伤区域血液流速和流量降低。同时,血小板们接触到破损处血管内皮下的胶原蛋白,被迅速激活,快速地聚集到破损处,从圆盘状变为球形,并形成丝状伪足。丝状伪足像胳膊一样,使得血小板可以彼此拥抱,凝成一团,形成血小板血栓。
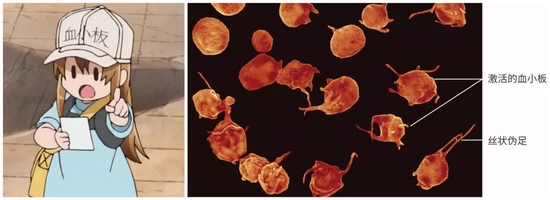 左:《工作细胞》中拟人化的血小板右:实际的血小板与血小板的激活|John Weisel, PhD, Perelman School of Medicine, University of Pennsylvania
左:《工作细胞》中拟人化的血小板右:实际的血小板与血小板的激活|John Weisel, PhD, Perelman School of Medicine, University of Pennsylvania但血小板血栓仅仅是血管上的一个“临时创口贴”,要真正完全止血,并为受损的组织提供修复时间,就需要经历一串复杂的生理过程,形成一道更加牢固的“墙”。
人体血液中含有十余种凝血因子,在受伤出血后,它们就会被依次激活,形成一个复杂的反应链,这个过程中,出血的信号会被一步步放大,最终激活血液中的凝血酶原变成凝血酶。
在凝血酶的催化下,血液中原本可溶性的纤维蛋白原转变为不可溶的纤维蛋白,它们彼此连接,形成网状,将血小板血栓和一些血细胞网罗其中,使血液失去流动性,变成胶冻状的凝块,从而完成止血的核心步骤。
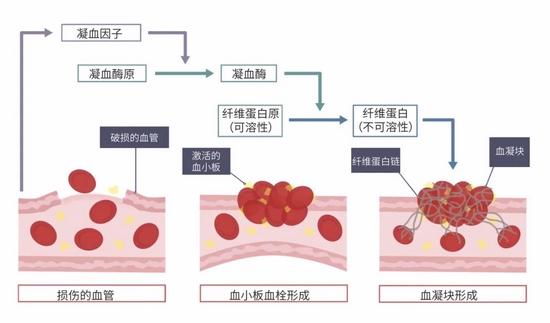 凝血因子级联反应形成纤维蛋白网 | http://igcse-biology-2017.blogspot.com/2017/06/264b-understand-how-platelets-are.html,作者汉化
凝血因子级联反应形成纤维蛋白网 | http://igcse-biology-2017.blogspot.com/2017/06/264b-understand-how-platelets-are.html,作者汉化然而,当出血量非常大时,单凭我们自己的凝血功能,没有办法在短时间聚集起大量的凝血酶和纤维蛋白到达出血部位。血液在瞬间大量流失可能危及生命,能否快速止血就是决定生死的关键,这时就要依靠一些药物或者外科手段,来应对大量出血。
利用毒蛇毒液提取物止血
毒蛇,在我们的印象中,可能是海蛇、尖吻蝮、 眼镜王蛇、 舟山眼镜蛇、明楼这类可怖的生物。然而科学家发现,虽然毒蛇的毒液中含有作用于神经系统和血液系统的毒素,但其中一些有效成分可能也是类似凝血酶的救命“神器”。
早在1936年,科学家就从美洲矛头蝮(Bothrops jararaca)的毒液中分离出了可以促进凝血的成分——血凝酶。1937年,科学家发现多种蛇的毒液能让血浆发生凝集,其中就包括来自矛头腹蛇(Bothrops atrox)的毒液。1954年,一家瑞士制药公司对矛头蝮蛇的毒液进行分离,从中提取出了具有凝血作用的爬虫酶(又称巴曲酶)。
后续研究发现,爬虫酶的作用方式与人体中的凝血酶类似,可将纤维蛋白原转化为纤维蛋白单体,进而形成多聚化的纤维蛋白网络。
而后这种药物,被广泛地运用到临床当中,既可以在手术前使用预防性地降低手术风险,也能在手术后使用帮助伤口止血。
 矛头腹丨Wikimedia Commons,Alex Kwok/CC BY-SA 3.0(https://creativecommons.org/licenses/by-sa/3.0)
矛头腹丨Wikimedia Commons,Alex Kwok/CC BY-SA 3.0(https://creativecommons.org/licenses/by-sa/3.0)凝胶闭合伤口,阻断出血源头
除了增强凝血,将开放的伤口闭合也是防止血液大量流失的根本,而我们人体血液中的组织粘合剂就是发挥闭合伤口的作用的。顾名思义,粘合剂就像胶水,将其涂在伤患血管的破损处,它就像能把破损的地方重新封闭起来,从而达到止血的作用。
粘合剂可分为天然组织粘合剂和合成性组织粘合剂。天然的组织粘合剂因为低毒性、生物适应性比较好而更受欢迎,多糖、胶原蛋白、白蛋白等都可以作为天然组织粘合剂的原料。但这些物质也有一个很大的弱点——力学强度有限,尤其是在很湿的组织表面上粘附性很差。因此,当天然组织粘合剂遇到大量出血,粘合效果就会大打折扣。
针对这种缺陷,2019年来自浙江大学的研究团队对组织黏合剂进行改良,通过添加糖类增强了它的力学强度,同时加入具有光反应性的基团,制成甲基丙烯酰基明胶(GelMA),将其和其他生物大分子混合做出水凝胶。这种材料不仅可以应对出血量较大的情况,还可以在紫外线的照射下,使明胶上的甲基丙烯酰基快速手牵手,形成凝胶,粘附在流血的血管上并把伤口封闭住。
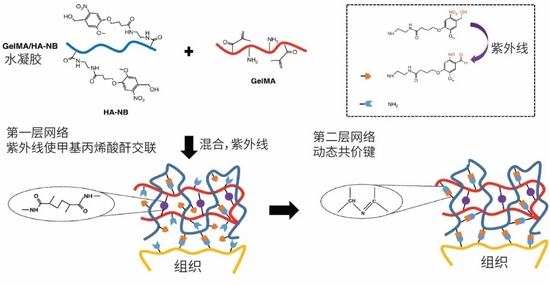 紫外光激活,快速形成水凝胶
紫外光激活,快速形成水凝胶凝胶+蛇毒,止血效果up
使用GelMA技术,紫外线照射的一大问题就是会造成DNA损伤和突变。如果仅用可见光就能激活粘合剂的交联,那么不仅可以降低组织的损伤,还能提供细胞的成活率。
2021年7月,一项新研究发布在《科学进展》中,研究人员在GelMA中加入了三乙醇胺、N-乙烯基己内酰胺和伊红Y,实现了在430~530 nm可见光的短暂照射下就让GelMA发生交联,形成凝胶,扩大了这种组织粘合剂的应用场景。科学家们称,一只激光笔甚至是手机的手电就可以让药物迅速发挥作用,闭合伤口。
 430~530 nm可见光激光笔即可以激活HAD形成水凝胶
430~530 nm可见光激光笔即可以激活HAD形成水凝胶但是由于GelMA本身的止血效果较弱,对于严重出血的病例可能帮助非常有限,为了克服这个缺点,科学家们受到了矛头蝮蛇毒的启发,向GelMA中加入爬虫酶,各取所长,制成了这种既可以在可见光下迅速发生交联,在伤口处形成物理屏障,又可以加速纤维蛋白网形成的全新止血粘合剂HAD。
研究中,科学家们对这款HAD进行了全方位的测试。
在粘附强度测试中,它的粘附强度几乎是市售组织粘合剂纤维蛋白胶水的10倍。体外的凝血测试中,科学家们使用没有血小板的血浆,测试在没有干预的条件下,血液凝固时间在5-6分钟, 使用纤维蛋白胶水可大大降低凝固时间到约1分30秒,而使用这种最新型HAD粘合剂血液凝固只需约45秒。
在实验动物体内,科学家们使用了四种不同的出血模型,来模拟不同的受伤场景,并对出血量和凝血的时间进行了测定。
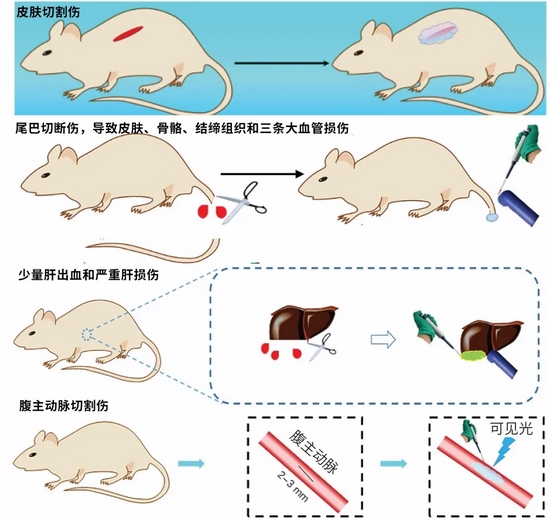 对HAD进行在体测试的4个受伤场景
对HAD进行在体测试的4个受伤场景在所有模型中,HAD均可以显著加速皮肤伤口的关闭,并在血管非常丰富的组织中,将失血量和凝血时间均降低约50%。
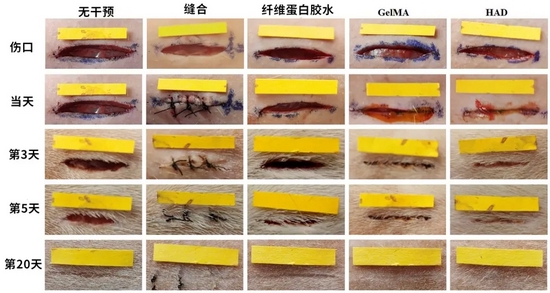 多种方法处理皮肤切割伤的对比图
多种方法处理皮肤切割伤的对比图根据电子显微镜对于伤口处的观察,研究者提出了HAD发挥作用的模型:当HAD的成胶前溶液与受伤组织接触的时候,首先发生扩散和渗透,与组织的界面充分接触。在经过光的激活后,HAD迅速多聚化,产生的多聚物与组织交织在一起,形成了互锁结构。
HAD中的GelMA促进血小板和红细胞的聚集和激活,与此同时其中的爬虫酶快速触发纤维蛋白原向纤维蛋白的转化。最后,血小板的丝状伪足可以拉住纤维蛋白的纤维,并使其弯曲,产生张力,使得凝血块收缩,形成力学上稳定的结构,从而达到完全止血。在整个过程中,GelMA和爬虫酶各司其职,又彼此协同,从而使HAD达到了极佳的止血效果。
HAD研究的负责人之一基布雷特·麦昆尼特(Kibret Mequanint)教授表示,下一步就是要将HAD这项研究成果转化并推广到临床上。爬虫酶这款已经在市场上存在了60余年的老药,又要与GelMA合作共同作战,应对伤口出血。
或许不久后,我们就会在家庭急救箱中发现这款HAD凝胶的踪影,当然,旁边还会搭配一只激活药物开关的激光笔。
相关文章
猜你喜欢
今日头条
图文推荐
精彩文章
随机推荐